miRNA的作用机制
miRNA 在发挥作用之前,需要同细胞内Germin3、Germin4和Argonaute蛋白家族成员eIF2C2因子等协同因子结合形成蛋白质-RNA复合物(miRNA-containing ribonucleic protein,miRNP),在miRNP的作用下指导其识别同源mRNA,研究认为miRNP即为RISC,并引起靶mRNA的降解或翻译的抑制。
当RISC复合体与miRNA的向导链结合之后,便进行mRNA的识别。绝大部分RISC复合体与靶标mRNA之间的结合能(binding energy)都来自于miRNA种子区的核苷酸。即RISC复合体之所以能够被靶标识别并结合主要是因为RISC具有固有的、非特异性的亲和力。但是,靶标的可结合性是直接与其降解效率相关的,这说明RISC复合体并不能够打开RNA分子的二级结构。
在细胞内,mRNA分子均与核蛋白(ribonucleoproteins,RNP)结合在一起,以复合体的形式存在,因此mRNA分子的可识别性还会受到几种RNA结合蛋白的影响,因为这些蛋白有可能会遮蔽mRNA分子的结合位点或者打开mRNA的二级结构。因此,RISC复合体的作用似乎就是根据结合的靶标而定的。它的作用模式不仅会受到靶标mRNA分子上用来与miRNA结合的位点结构的影响,还会受到与每一个Argonaute蛋白结合的RNA结合蛋白的影响。比如,在动物体内,miRNA至少可以通过作用于靶mRNA 3’端非翻译区里的结合位点的三条各不相同的途径来沉默基因表达(切割mRNA靶标分子、抑制mRNA靶标分子的翻译表达,或降解mRNA靶标分子)。
不过,对于每一个单独的miRNA-mRNA沉默复合体来说,由抑制翻译和直接降解而造成的基因沉默效果并不相同。此外,最终的沉默效果可能还会受到其他能够与靶mRNA或RISC复合体发生相互作用、抵消miRNA的蛋白质的影响。这样,每种组织因其所含蛋白的不同,导致了完全不同的调控结果。
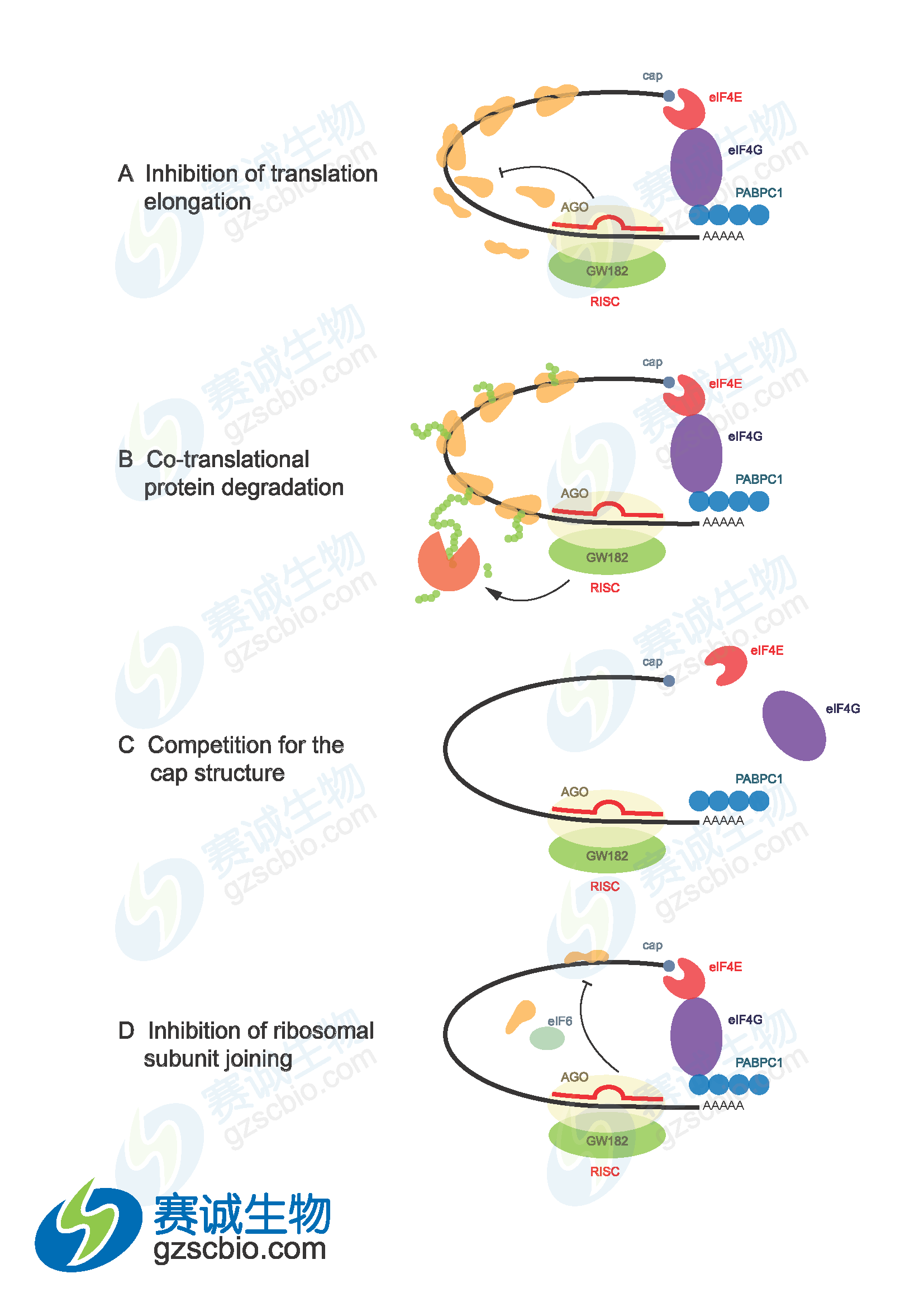
图1 miRNA介导基因沉默机制
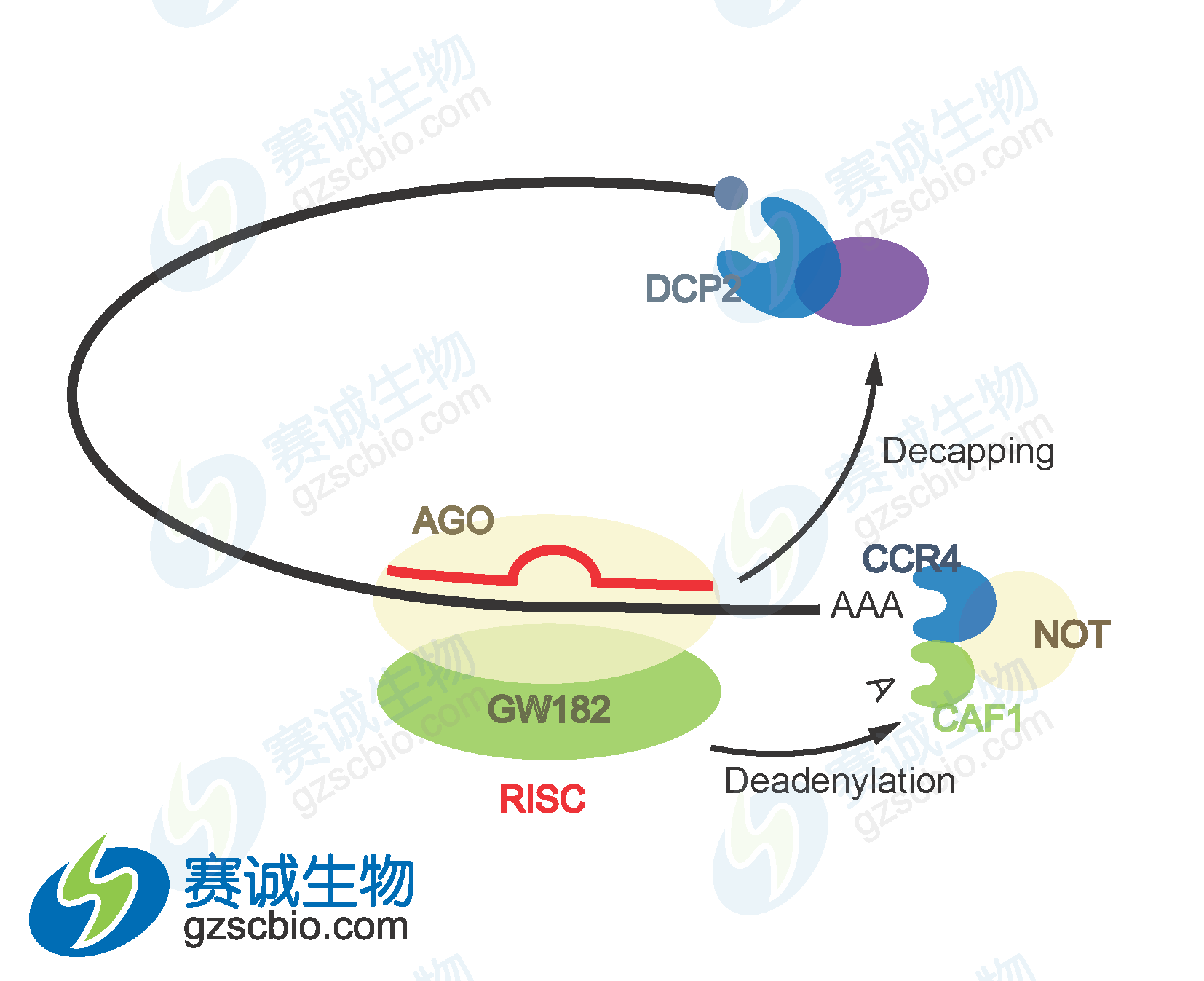
图2 miRNA接到信使RNA降解
miRNA对靶基因的调控表现在转录后水平上,通过对靶基因mRNA的切割或对其翻译抑制两种机制来下调靶基因的表达。这两种机制的选择主要取决于它与靶基因mRNA序列互补的程度,如果miRNA与靶基因mRNA完全互补,miRNA将通过切割方式来调控靶基因;如果miRNA与靶基因mRNA不完全互补,miRNA将通过翻译抑制的方式来调控靶基因;并且对靶基因翻译的抑制可能需要多种miRNA分子的协同作用。在动物体内,大部分miRNA不能与靶基因的mRNA完全互补,故被认为主要通过翻译抑制的方式来调控靶基因。
在大多数情况下包括人类,大多数动物复合物中的成熟miRNA与靶基因mRNA 3’端非翻译区(untranslated region,UTR)不完全互补配对,在转录后水平抑制靶基因的表达,抑制该基因的翻译过程,从而抑制基因的表达。
miRNA 以4种不同的方式抑制蛋白质表达:(1)与翻译偶联的蛋白质降解;(2)翻译延长的抑制;(3)翻译提前终止(核糖体脱落);(4)翻译起始的抑制。另外,尽管有不完全的mRNA-miRNA碱基配对,动物miRNA能够诱导mRNA靶基因大量降解。微RNA还可以在称为mRNA 加工体或P体(不存在翻译机制)的独立细胞质位点,通过螯合mRNA 使其沉默。miRNA 是否进行mRNA降解主要取决于miRNA 结合位点和RNA 环境的特定性质,最可能的决定因素是miRNA与特定标靶结合蛋白的特殊相互作用。miRNA可以与Ago2结合,将与它们结合的靶基因 mRNA 转移到并富集于细胞质的某一部位,在那里mRNA被破坏,这个部位被称为P小体,P体的其他组分,如GW182、CAF-CCR4-NOT脱腺苷酶复合物、脱帽酶DCP2、脱帽激活因子(如 DCP-1、EDC3、Ge-1)和RNA解旋酶RCK/p54 等都参与miRNA功能。
另一方面,当miRNA与mRNA完全互补配对时,则引起目的基因mRNA在互补区的特异性断裂,从而导致基因沉默,这种miRNA对靶基因mRNA的切割对靶基因mRNA的切割是大多数植物、病毒和部分动物的miRNA调控靶基因的主要方式。miRNA可以指导对靶基因mRNA的多次切割而本身保持完整,这种作用方式与siRNA类似,miRNA对基因的调控也是通过构成RISC来进行的,RISC是其调控的物质基础。RISC组成的核心成分是miRNA或siRNA以及各种蛋白,其中Ago蛋白是该复合体中的核心蛋白,具有非常重要的作用。